中科院上海药物研究所苏州药物研究院优势
中科院上海药物研究所苏州药物研究院分析测试中心,2013年11月18号成立,拥有核磁(NMR),气相色谱-质谱联用检测仪(GC-MS)、液相色谱-三重四极杆质谱联用检测仪(LC-MS)、电感耦合等离子体发射光谱仪(ICP-OES)、电感耦合等离子体质谱仪(ICP-MS)、高效液相色谱仪(HPLC)、气相色谱仪(GC)、元素分析仪,离子色谱,全自动溶出仪、微波消解/萃取系统等数十种各种高端检测仪器设备,并已经通过实验室计量认证(CMA)。以这些先进的设施设备为基础,公司目前已经具备了承担参比制剂逆向剖析、微量杂质分析、药品包材相容性研究、基因毒性杂质研究,药学质量研究等检测分析及研究开发的技术平台。
主要研究方向 包括 制剂逆向工程,原辅料剖析,处方工艺开发,基因毒性杂质研究,包材相容性研究,大型仪器测试。
业务范围
1、成品和原液药包材相容性研究,包括:西林瓶、安瓿瓶、胶塞、预灌封、滴眼剂瓶、塑料瓶、细胞冻存袋、塑料桶、不锈钢桶。
2、生产过程组件相容性研究,包括:硅胶管、过滤器、连接组件、玻璃组件、不锈钢组件、储液袋、搅拌袋。
3、医疗器械材料化学性,包括:气体管路测试、化学表征可滤物等材料化学特性研究
4、给药器具相容性研究,包括:输液器、注射器、留置针、一次性给药适配器等给药器的相容性研究
包材相容性流程研究
1、信息的收集评估:
根据项目申请单的包装材料配方信息、生产工艺信息以及药品有关的关键参数(如规格、给药途径、日摄入量等)为客户定制相容性研究方案
2、提取实验和模拟试验
模拟、提取试验会充分考虑药品在生产、贮存、运输以及使用过程中可能面临的极端条件进行阈值的计算、模拟液和模拟条件的选择,以及对可提取物方法的开发,帮助客户筛选包材
3、浸出物(迁移)实验
针对加速、长期稳定性样品的测试,根据NMPA药品检测试验记录规定规范原始数据管理
4、方法学设计与验证
根据中国药典、美国药典和国内相关指导原则,对检测方法进行方法学验证,内容包含但不限于专属性、线性、系统适用性、准确度、精密度(重复性和中间密度)、检出限和定量限
5、毒理学安全性评估
参考毒理学数据库如DEREK,TOXNET,HSDB,TOXLINE等,由毒理学专家完成包括建模、数据库查询、文献查询、阈值计算等工作,从而得到完整的毒理学评估报告。
6、结论
结合可提取物研究和浸出物研究结果,并参考毒理学评估结果,给出终的相容性研究结论
包材风险分类

包材相容性流程研究流程图
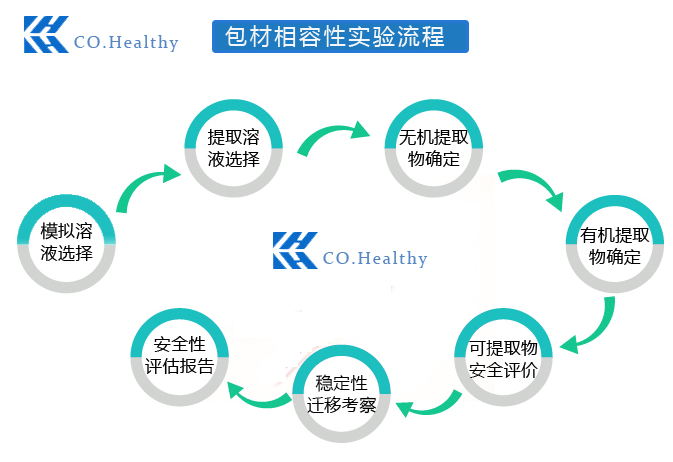
参考的国内法规如下
《化学药品注射剂与药用玻璃包装容器相容性研究技术指导原则(试行)》
《化学药品注射剂与塑料包装材料相容性研究技术指导原则(试行)》
《化学药品注射剂与药用弹性体相容性研究技术指导原则(试行)》
《YBB00142002-2015药品包装材料与药物相容性实验指导原则》
《中国药典》2015版等
PQRI
ICH Q3D
USP 1663&USP1664
USP 665& USP 1665
常见问题
包装材料和药品种类多样、复杂
法规要求理解不透彻,无法设计出一套完整的解决方案
溶出量极低且体系复杂,仪器的高灵敏度和高选择性并重